 La AEMPS ha emitido una nota informativa sobre las restricciones provisionales de uso aplicadas al tofacitinib a raíz de la difusión de los resultados preliminares de un ensayo clínico actualmente en curso, que mostraron un aumento del riesgo de embolia pulmonar (EP) y mortalidad global en los pacientes tratados.
La AEMPS ha emitido una nota informativa sobre las restricciones provisionales de uso aplicadas al tofacitinib a raíz de la difusión de los resultados preliminares de un ensayo clínico actualmente en curso, que mostraron un aumento del riesgo de embolia pulmonar (EP) y mortalidad global en los pacientes tratados.
Se trata de un ensayo clínico diseñado para evaluar la seguridad de tofacitinib 5
mg y 10 mg dos veces al día en comparación con inhibidores del factor de
necrosis tumoral (anti-TNF), en pacientes con artritis reumatoide. Se observaron 19 casos de EP en 3.883 años-paciente de tratamiento en el grupo tratado con 10 mg cada 12 h de tofacitinib, en comparación con 3 casos de EP en 3.982 años paciente en el grupo tratado con anti-TNF. Adicionalmente, hubo 45 casos de muerte por cualquier causa en 3.897 años-paciente en el grupo tratado con tofacitinib comparado con 25 casos en 3.982 años paciente en el grupo tratado con anti-TNF.
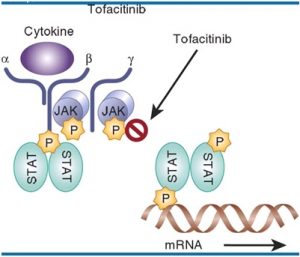 El tofacitinib es un inhibidor selectivo de la familia de las JAK, enzimas encargadas de la transducción de la señal intracelular desde los receptores de la superficie celular para ciertas citocinas y factores de crecimiento, y activadores de la transcripción. Inhibe de manera preferente JAK1 y JAK3 y con menos potencia para JAK2 o TYK2, lo que reduce las señales de interleucinas y interferones, modulando así la respuesta inflamatoria e inmune. Está aprobado para el tratamiento de la artritis reumatoide, la artritis psoriásica y la colitis ulcerosa.
El tofacitinib es un inhibidor selectivo de la familia de las JAK, enzimas encargadas de la transducción de la señal intracelular desde los receptores de la superficie celular para ciertas citocinas y factores de crecimiento, y activadores de la transcripción. Inhibe de manera preferente JAK1 y JAK3 y con menos potencia para JAK2 o TYK2, lo que reduce las señales de interleucinas y interferones, modulando así la respuesta inflamatoria e inmune. Está aprobado para el tratamiento de la artritis reumatoide, la artritis psoriásica y la colitis ulcerosa.
Mientras se lleva a cabo la revisión del balance beneficio-riesgo y hasta que se conozcan las conclusiones definitivas de la misma, la AEMPS informa a los profesionales sanitarios de las medidas provisionales y las recomendaciones establecidas en una nota informativa.

